![]()
|
| 3 新しいニパウイルス感染症の発生 マレーシアの発生で完全に消滅したかに思われたニパウイルス感染症は,バングラデシュで発生した.バングラデシュにおけるニパウイルス感染症の最初の発生は2001年4月から5月にかけて起こり,この時の発生では25名が感染し7名が死亡しており,2名の患者からニパウイルスに対する抗体が検出されている.この発生では患者との接触による人から人への感染により疾病が広がったと報告されている.この発生の前,2000年10月から11月にかけてインドの北ベンガル地方で年齢3〜12歳の112名の子供が感染し,43名が死亡し,米国疾病対策センター(CDC : Center for Diseases Control and Prevention)に送った6サンプルからニパウイルスに対する抗体が検出されている.バングラデシュの最初の発生地はインド国境に近く,インドの発生と関連があるものと考えられた.続いて2003年1月にはバングラデシュのNaogaon地区Chalsita村及びBiljoania村で新たな発生が認められ,17名が感染して,8名が死亡し,4名の患者からニパウイルスに対する抗体が検出された.2004年1月から2月にかけて,Rajibali,Faridpur,Golgaganji,Manikganji,Joypurat及びNaogaonの6つの地域でニパウイルス脳炎が発生した.この時の致死率は74%と高く,23名が感染し16名が死亡している.このうち,11名の患者からニパウイルスに対する抗体が検出され,2名の患者からマレーシアで分離されたニパウイルスと95%の核酸の相同性を示すウイルスが分離された.そして,2004年3月には再度Faridpur地区で大きな発生が見られた.致死率は79%と今までで最も高く,34名が感染し,27名が死亡している.この発生では21名の患者からニパウイルスに対する抗体が検出された.2005年1月にはTangail地区のBasail Upzilaで高熱と神経症状を示し,1週間以内に8名が死亡した(図2)[8]. これらの発生で注目されたことは,家族内での人から人への感染である.患者の多くは初期に呼吸器症状を示していたが,これを裏付けるようにニパウイルス脳炎の患者の胸部レントゲン写真は肺炎像を示していた[8]. 2004年3月の発生地Faridpurにはオオコウモリ(インドオオコウモリ:Pteropus giganteus )が生息し,このオオコウモリからニパウイルスに対する抗体が検出されている.この地区では子供たちがジャングルに入り果実を取ってきて食べる習慣があり,オオコウモリが食しウイルスに汚染された果実を食べて感染したのではないかと考えられている.とにかく,バングラデシュのニパウイルス感染症の発生で,マレーシアの発生と大きく異なる点は,マレーシアの時のようにウイルスを増幅させる動物(豚)の介在がないこと,患者の肺炎像が顕著で,人から人への感染が明らかに認められることがあげられる[8].この肺炎病巣はマレーシアでの発生でも少数認められたが,人から人への感染は認められなかった[9]. このように,マレーシアにおける発生のみで終息したかにみえたニパウイルス感染症が,その後感染様式を変え,別の国で発生したのである.そして2007年にインドの西ベンガル州(州都カルカッタ)のNadia地区(カルカッタの北)で発生し少なくとも30名が発症し3名が死亡したことが5月7日に報告された(ProMed-mail: http://www.promedmail.org).2007年2月頃から同様の疾病で50名の発症者があり5名が死亡しており,この発生に関連があるとされている.西ベンガル州はバングラデシュのすぐ隣で,この地域にはオオコウモリが多数生息しておりニパウイルス感染症の新たな発生として注目される. |
| 4 再発症もしくは遅発症するニパウイルス感染症 再発性ニパウイルス脳炎とは急性脳炎を併発し,回復した患者が再び顕著な神経症を併発するもので,遅発性ニパウイルス脳炎とは最初の感染では不顕性感染で症状を示さなかった人が,10週間以上経過し脳炎を併発するものである.急性脳炎の脳病巣はCTスキャンでは小さなハッキリとした病巣として観察されるが,再発性及び遅発性脳炎では広範囲の病巣として観察される.ニパウイルス感染患者のその後の経過観察記録から,再発性ニパウイルス脳炎は急性脳炎を併発した患者の9%(14名)で認められており,遅発性ニパウイルス脳炎は症状を示さなかった感染者の5%(11名)に認められている.再発もしくは遅発性で脳炎を発症するまでの期間は平均13カ月で,最長の人は4年半にも及ぶとの報告がなされており,ニパウイルスに一度感染すると,その時は不顕性感染や,症状が回復したとしても,1年以上経って再発が起きるのである[10]. このように,ニパウイルス感染症が長い年月を経て発症もしくは再発するのであれば,回復した人や,当初発症せず,日常生活を送っていた人が突如発症し,ニパウイルスの感染源になりうることも考えられる.この点は,マレーシアのニパウイルス感染症発生当時に多くの人が出稼ぎに来ていたと考えられるバングラデシュでニパウイルス感染症が発生していることの関連において興味深い. |
| 5 お わ り に マレーシア及びバングラデシュ両国の発生疫学より,ニパウイルス感染症はジャングルに生息するオオコウモリから豚に感染,もしくは直接コウモリ自身から感染したものと考えられている.今まであまり注目されていなかったオオコウモリが,新興共通感染症の自然宿主として脚光を浴びてきたのである.しかし,オオコウモリは危険な動物であり,淘汰しなければいけないという考えを持つ人が出てくると困るので,なぜこのような事態になってきたのか再度述べておく. オオコウモリ固有のウイルスが家畜もしくは人に感染するようになった最大の理由は,人間による自然破壊である.人間が彼らの住処や餌場を開発のために消滅させていったことが大きな原因で,また人間が大量に排出する二酸化炭素により地球温暖化を促進し,異常気象が頻繁に現れるようになり,ジャングルの果樹が育たたなくなり,彼らの餌がなくなったことも大きな要因である.そのほか,近年のペットブームで多種多様な,いわゆるエキゾチックアニマルを人間が求めるようになり,珍しい野生動物を捕獲するようになったことや,空前のグルメブームにより珍しい食材を求め,さまざまな野生動物を捕獲するようになり,これらの動物との接触機会が増加したことも要因と考えられる.この珍しい食材の中にはオオコウモリが入っており,東南アジアでは観光客が珍味として食べることがあるようである.しかし,カンボジアのレストランで食用に捕獲されたライルオオコウモリ(Pteropus lylei )からはニパウイルスに対する抗体が検出され,ニパウイルスも分離されている[11]. 2003年に突如出現し,多くの人が感染し死亡したSARS(Sever Acute Respiratory Syndrome:重症急性呼吸器症候群)の最初の感染源は広東料理の珍味として捕獲されていたハクビシンといわれていた[12].その後,ハクビシンも被害者で,SARSウイルスの宿主は食虫コウモリであるキクガシラコウモリとの見解が出された[12].しかし人間にSARSを感染させたのは食材として捕獲されたハクビシンである. ニパウイルス感染症の出現理由について,いろいろ考察を行ったが,上記のようにすべて人類のエゴが招いたものと結論づけられる.人類は,今一度自身のエゴを戒め,共存ということを真剣に考える時期に来ている.このままこの状況を放置すれば,奢ったわがままな人類への天罰という形で,今後さまざまな新しい共通感染症が出現してくるであろう. |
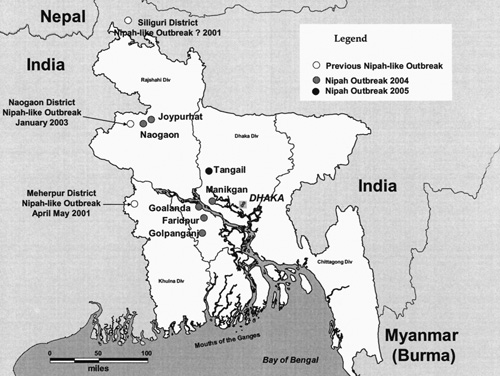 (マラヤ大学医学部C.T.Tan教授のバングラデシュ調査報告より改変) 図2 バングラデシュにおけるニパウイルス感染症の発生状況.○の地域が2001年〜2003年までの発生地域で,は2004年の発生地域,そして●で示された場所が2005年の発生地区. |
| 引 用 文 献 | ||||||||||||||||||||||||
|
| † 連絡責任者: | 白井淳資(東京農工大学大学院共生科学技術研究院) 〒183-8509 府中市幸町3-5-8 TEL・FAX 042-367-5780 E-mail : jshirai@cc.tuat.ac.jp |