|
家畜衛生研修会(病性鑑定病理部門,2002)*†
における事例記録(III)
Proceedings of the Slide-Seminar held by the Livestock Sanitation Study Group
in 2002*†, PartIII
(2003年4月1日受付・2003年6月3日受理)
| 〈事例報告No. 15〜23(前号)から続く〉 | ||
事 例 報 告 |
||
| 24.牛の亜急性壊死性肝炎 | ||
〔鎌田博志(宮崎県)〕 |
||
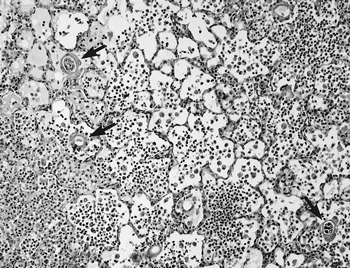
| 黒毛和種,雄,120日齢,斃死例(死後約1時間で剖検).繁殖牛16頭と産子13頭を飼養する生産農家で,2001年10月から11月にかけ生後約120日齢の子牛3頭が,横臥,四肢伸張,振戦および眼球振盪を呈して斃死した. 剖検では,肝臓は全体に暗赤色を呈し,大豆大から拇指頭大の褐色斑が数カ所認められた.また,肺にうっ血および軽度の胸膜炎があった. 組織学的には,肝臓ではびまん性,小葉中心性に重度の肝細胞壊死・脱落があり,肝細胞の脱落部には赤血球とマクロファージ系細胞が充満していた(図24).中間帯には好酸性の滴状物を容れる球状物やマクロファージ系細胞が散見され,小葉辺縁部では肝細胞の再生,胆管の増生と偽胆管の形成が認められた.好酸性滴状物の同定のために銅,亜鉛,鉄およびマンガンなど微量金属による過酸化反応にともなうNitrotyrosinの免疫組織化学的検出をこころみたが陰性で,PAS反応,PTAH,ベルリンブルーも陰性であった.大脳では,皮質において神経細胞の壊死と神経網の空胞化および血管周囲腔の拡張がみられた.同様に病性鑑定を行った他の1例についても,肝臓と大脳に同様の組織所見が認められた. 病原検索では,主要臓器から細菌は分離されなかった.血清生化学的検査では,TP 6.5g/dL,AST 634KU,γ-GTP 122IU/L,ALP 182KAU,CPK 802IU/Lと肝機能障害が示唆され,BUNなどは正常範囲内であった. 以上から,本症例は病理組織学的に中毒が疑われたが,免疫組織化学的検出法によって微量金属を検出できず,原因物質の特定にいたらなかった. |
||
|
||
| 25.ハクビシンの肝臓における結節性過形成,再生結節および肝細胞癌 | ||
〔小桜利恵(富山県)〕 |
||
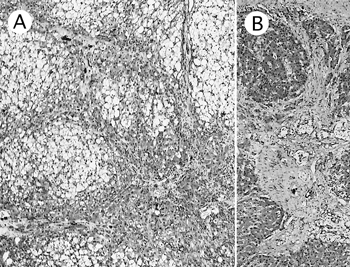
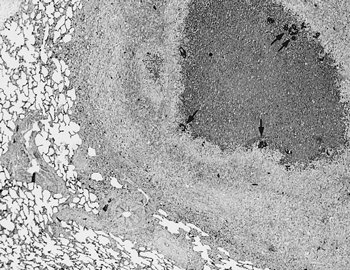
| ハクビシン,雌,21歳以上,斃死例(死後2日で剖検).動物園で展示飼育されていたハクビシンが,元気消沈,腹部膨満および尾端部脱毛を呈し,約1カ月後に斃死した. 剖検では,肝臓に6×3×3cmで凹凸のある不整形腫瘤と灰白色〜赤褐色の6×6×5cmの楕円形腫瘤がみられた.不整形腫瘤は楕円形腫瘤と接し,さらに楕円形腫瘤は外および内側右葉と接していたが,それぞれの境界は明瞭であった.不整形腫瘤の割面では白色の結節が,楕円形腫瘤では灰白色ないし赤褐色で大小の結節が認められた.肝臓は横隔膜と癒着し,腹腔には乳赤色の腹水が大量に貯留していた. 組織学的には,不整形腫瘤ではおもに肝細胞様細胞の境界明瞭な腫瘍性増殖巣がみられ,血管様管腔構造を含むが胆管を欠く結合織で分画されていた.腫瘍細胞は,クロマチンに乏しい明るい核と泡沫状の豊富な細胞質をもち,大小不同で核・細胞質比は不定,充実性の腺房構造をとっていた(図25A).免疫組織化学的には肝細胞マーカー(HepPara1,DAKO社)陽性を示した. 一方,楕円形腫瘤部では腫大した肝細胞の結節性増生がみられた(結節性過形成).小葉構造は不規則で,肝細胞は2列あるいは島状に配列していた.また,一部で巣状の線維化,小葉間結合織の線維性肥厚,偽胆管の増生およびブリッジ形成(図25B)をともなった肝細胞の増生や巣状壊死が認められ,これらは肝細胞傷害に対する反応性の変化と考えられた(再生結節). 以上から,結節性過形成,再生結節および肝細胞癌と診断した.これらの病変の関連性に興味がもたれ,まれな症例と考えられた. |
||
|
||
| 26.鶏の肝臓にみられた未分化肉腫 | ||
〔平井伸明(岡山県)〕 |
||
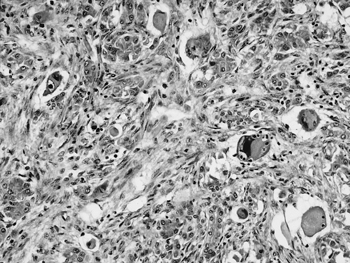
| チャンキー種,雌,56日齢.2001年9月,食鳥処理施設でブロイラーの肝臓に白色結節が認められた.臨床的な異常は観察されていなかった. 剖検では,肝臓の全域にわたり,大豆大の白色で表面の円滑な卵円形腫瘤が密発していた.筋胃の漿膜面に同様の白色腫瘤が認められ,肺にも白色巣が密発していた. 組織学的には,肝臓実質内に紡錘形から線維芽細胞様の細胞や弱好酸性の細胞質をもつ大型,類円形ないし多形性の細胞が腫瘍性に増殖していた(図26).大型の腫瘍細胞は楕円形の淡明な核を有し,核膜および核小体が比較的明瞭であった.多核巨細胞も散在し,ときおり細胞質内に偽好酸球,リンパ球等を貪食した像も認められた.腫瘍細胞は一部PAS反応陽性,免疫組織学的にはデスミン陽性を示した.PTAH染色では細胞質内線維や横紋は確認できなかった.筋胃では筋層間に同様の巣状増殖があり,筋胃の筋線維が腫瘍細胞間に巻き込まれる像も認められた.肺にも同様の腫瘍性細胞増殖があり,腫瘍と肺の間質との境界は不明瞭であった. 本症例では腫瘍細胞種の特定にいたらず,未分化肉腫と診断された. |
||
|
||
| 27.養殖ヒラメにみられたビブリオによる肝臓の多発性巣状壊死 | ||
〔田中宏一(香川県)〕 |
||
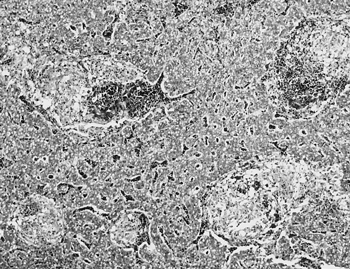
| ヒラメ,雄,約12カ月齢,斃死例(死後6時間以内に剖検).養殖用ヒラメを1小割5,000尾で1イケス約20,000尾飼養している養殖場で,2000年10月に急激な気温の上昇とともに1日約300尾程度のヒラメが体背部の潰瘍,ヒレのびらんを呈して死亡した.10月31日〜11月1日に体表の潰瘍を呈し死亡した養殖用ヒラメ8尾(2小割,2日間)について病性鑑定を実施した. 剖検では,無色透明な腹水が中等度に貯留していた.体表に約2×2cmの出血をともなった潰瘍,ヒレにびらん,エラに出血・白斑がみられた.肝臓,脾臓および腎臓には米粒大の白斑が認められ,脾臓は腫大していた. 組織学的に,肝臓に小型円形細胞やマクロファージの浸潤をともなうび漫性巣状壊死が認められ,肝細胞は混濁腫脹および脂肪変性を呈していた(図27).脾臓に出血をともなった巣状壊死,腎臓に多発性巣状壊死が確認され,ともに細網細胞やマクロファージの増生が認められた.心臓は心筋線維間質に組織球様細胞の浸潤と軽度の出血およびマクロファージの浸潤による心外膜炎が確認された.エラ・ヒレには出血,びらんおよび上皮細胞の増生,鰓薄板には小型円形細胞,マクロファージおよび好中球の浸潤が確認され,化膿性エラ炎,びらんをともなった化膿性ヒレ炎を呈していた.皮膚は潰瘍を呈し,出血およびマクロファージの浸潤が認められた.その他,消化器官に著変は認められず,PAS染色で寄生虫等の寄生も認められなかった. 病原検索で,主要臓器(肝,脾,腎および心),エラおよび皮膚潰瘍部からVibrio alginolyticus が分離された. 以上のことから,本症例を養殖ヒラメのビブリオ病と診断した.その後,緩やかな気温の低下とともに養殖用ヒラメの症状は回復した. |
||
|
||
| 28.Actinobacillus lignieresii 4型によるアステロイド体をともなった牛の化膿性肉芽腫性肺炎 | ||
〔亀山 衛(兵庫県)〕 |
||
| 黒毛和種,去勢雄,15カ月齢,鑑定殺.13カ月齢時に下顎部に直径約3cmの腫瘤が数個確認された.その後腫瘤は成長し,15カ月齢時には硬口蓋にも丘疹が認められ,採食困難となった.予後不良のため病性鑑定に供された. 剖検では,左側下顎部に直径約4cmおよび18×5cmの腫瘤がみられた.腫瘤は周囲と境界明瞭で骨との癒着はなく,割面は黄白色で膿瘍が形成されていた.耳下リンパ節および咽頭後リンパ節はともに腫大し,膿瘍が形成され,硬口蓋は全域が赤色,水腫状の丘疹を呈し腐敗臭を発していた.肺は全葉にわたって直径約2cmの灰白色硬結巣が散在し,病巣内部に膿を容れていた. 組織学的に,肺の病変部では結合織に囲まれた膿瘍が認められた.膿瘍の中心部にはグラム陰性短桿菌の集塊を含むアステロイド体が散見され,周囲に著しい好中球の集簇,マクロファージおよび類上皮細胞の集簇からなる肉芽腫の形成が認められた(図28).下顎部腫瘤,耳下腺リンパ節,咽頭後リンパ節および硬口蓋病変部にも同様の所見が認められた.免疫組織化学的検査では,ABC法により病変部のアステロイド体中心部の菌塊およびマクロファージ内に抗Actinobacillus lignieresii 4型兎血清(動物衛生研究所)に対する陽性抗原が確認された. 以上の所見から,本症例は牛のアクチノバチルス症と診断された. |
||
|
||
| 29.豚肺虫の寄生を認めた豚のカタル性気管支肺炎 | ||
〔津波 修(沖縄県)〕 |
||
| LWD種,性別不明,50日齢,鑑定殺.母豚22頭,肥育豚51頭を飼育する一貫経営農家で,2001年12月下旬頃から発熱,腹式呼吸および発咳を主徴とする離乳子豚の斃死が増加し,症状を呈した豚を鑑定殺した. 剖検で,肺は無気肺および肺気腫が混在し,モザイク様を呈していた.脾臓は軽度に腫大していた.その他の臓器に著変は認められなかった. 組織学的に,気管支および細気管支内に線虫が散見され,気管支周囲にはリンパ球が重度に浸潤,気管支腔には好中球の浸潤が認められた.肺胞内には好中球,マクロファージおよびリンパ球が中程度〜重度に浸潤し,マクロファージや多核巨細胞に貪食された含子虫卵が多数認められた(図29).肺胞中隔は軽度に水腫性で肺胞上皮細胞の腫大を認めるところもあった.一部の小葉間結合組織に水腫性の肥厚が認められた.肺胸膜では線維素が軽度に析出し,好中球およびリンパ球の浸潤が認められた.抗Pasteurella multocida抗体を用いたABC染色では,肺胞腔内の好中球に陽性抗原が認められた.腎臓では,間質においてリンパ球の軽度〜中程度の浸潤が認められた.肝臓では単核球の結節性の集簇が散見された. 病原検索では,肺および脳からPasteurella multocida が分離された. 血液検査では,白血球数の上昇(31,500/μl)が認められた. 本症例は,最近では発生が稀となった豚肺虫の寄生が認められた症例であり,菌分離および免疫染色によりPasteurella multocida 感染が認められたことより,豚肺虫とPasteurella multocida の混合感染症と診断された.なお,気管支周囲のリンパ球の浸潤についてはマイコプラズマの関与も疑われた. |
||
|
||