| 32.鶏のロイコチトゾーン性卵管炎 |
| 〔荒井眞弓(神奈川県)〕 |
ジュリア,雌,362日齢,鑑定殺.採卵鶏1,400羽を飼養する農家で,2000年7月中旬頃から4群中2群の鶏に元気消失,緑便,貧血がみられた.9月14日の検診時に発症鶏の病性鑑定を実施した.
剖検では,肝臓,腎臓,心臓の褪色,腎臓のうっ血,脾臓の腫大(30×25mm)がみられた.十二指腸漿膜面と腸間膜に出血,盲腸内腔に多量の緑便が認められた.
組織学的には,卵管膨大部の粘膜固有層に第2代シゾントがみられ,周囲にリンパ球,偽好酸球,異物巨細胞が浸潤していた(図32).メロゾイト放出後のシゾント壁の内腔にはマクロファージ,リンパ球,偽好酸球,異物巨細胞が侵入していた.絨毛先端は水腫を呈して腫大し,固有層や粘膜下織の静脈周囲に多数のリンパ球浸潤がみられた.さらに下織には漏出性出血も認められた.第2代シゾントは膨大部以外の卵管,心臓の左心内壁にも認められた.肺では多数のガメートサイトと血栓形成が認められた.その他,全身の静脈周囲にリンパ球浸潤が認められた.
病原検索では,血液塗抹でロイコチトゾーンの原虫が確認され,ゲル内沈降反応による抗体検査で10羽中10羽すべてが陽性であった.
本例は全身の静脈周囲にリンパ球浸潤が著明であったが,坐骨神経において神経線維間にリンパ球浸潤を認めず,静脈周囲のみの浸潤であったため,マレック病の関与は否定され,ロイコチトゾーン病と診断された. |
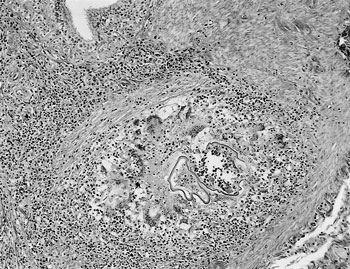
| 図32 |
鶏卵管膨大部の粘膜固有層の第2代シゾントと細胞浸潤(HE染色 ×100). |
|
| 33.大腸菌による子牛の化膿性髄膜脳炎 |
| 〔井上輝美(兵庫県)〕 |
黒毛和種,雌,6日齢,鑑定殺.成牛12頭を飼育する繁殖経営農家で,2000年5月2日生まれの子牛が起立不能となり,後弓反張等の神経症状を呈し予後不良と診断され,病性鑑定を実施した.
剖検では,大脳,小脳,延髄に線維素の付着がみられた.脳脊髄液は混濁していた.肺の一部に出血巣が確認された.
組織学的には,大脳,小脳および脊髄のくも膜下腔における好中球,マクロファージ主体の高度な細胞浸潤と線維素の沈着が顕著であった(図33).髄膜炎部付近の実質では炎症細胞浸潤により皮質と軟膜の境界が不明瞭で,神経網の粗鬆化がみられた.抗大腸菌ウサギ血清(DAKO)を用いた免疫組織化学染色により大脳,小脳,脊髄,肺,肝臓,脾臓,骨髄,眼球で陽性反応が検出された(取りまとめ担当者注:本血清と同一製品は免疫染色でサルモネラやリステリアとも交叉反応を示すことが確認されたので,血清の特異性についてさらに検討する必要がある).脾臓では白脾髄が減少し,胸腺ではび漫性に細胞密度が低下し,皮質リンパ球の減少が認められた.
病原検索では,大脳,脳脊髄液,肝臓,脾臓,心臓,肺,腎臓,臍帯から大腸菌が分離され,脳脊髄液では4.8×106CFU/mlであった.分離された大腸菌全株の生化学的性状ならびに薬剤感受性はすべて一致した.血液検査では,白血球数12,700/μl,血清総蛋白質量3.4g/dl,アルブミン
1.93g/dl,A/G比1.32,GGT 23U/l,γグロブリン欠損が確認され,初乳摂取不良が示唆された.
以上から本例は牛大腸菌症と診断された. |
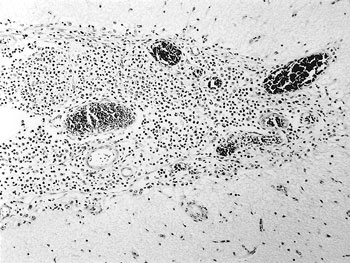
| 図33 |
好中球,マクロファージの浸潤(HE染色 ×100). |
|
| 34.牛の早産胎子にみられた接合菌による血栓性静脈炎の顕著な化膿性髄膜脳炎 |
| 〔佐藤勝哉(三重県)〕 |
黒毛和種,雌,0日齢(胎齢8カ月齢),死亡例(死後約1時間).繁殖雌牛250頭の一貫経営農場において,2001年6月15日群飼されていた母牛1頭が予定より約2カ月早く胎子を娩出した.娩出時の胎子の生死は不明であった.当該母牛は娩出時に子宮脱を起こし廃用となった.
剖検では,肝臓の表面,割面に粟粒〜小豆大の不整型の褪色巣が散在していた.大脳右半球前頭部冠状溝に接する実質において小指頭大の灰黄色巣が認められた.
組織学的には,大脳の前頭部にみられた灰黄色巣において,脳実質の神経網は粗造化し,リンパ球,好中球,単核細胞がびまん性に浸潤し,大脳皮質の固有構造は消失していた(図34).実質の小血管(静脈)内には線維素血栓が形成され,血管壁とその周囲にはリンパ球や好中球が浸潤していた.PAS反応,グロコット染色により,やや細い,無隔壁,分岐角不定の菌糸が認められ,血管とその付近に分布していた.同部位についてグラム染色,ギムザ染色を施したが細菌は確認できなかった.脳溝軟膜下から実質にかけてリンパ球が主体となって浸潤していた.肝臓では広範囲な凝固壊死巣が形成され,同部位にも菌糸が認められた.
病原検索では,主要臓器,脳から細菌は分離されなかった.
本例は,組織所見から牛の早産胎子にみられた接合菌症と診断され,まれな症例と考えられた. |
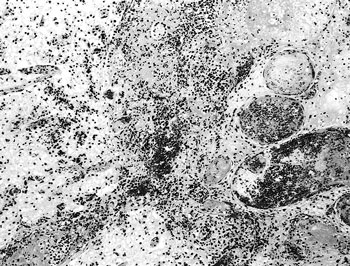
| 図34 |
静脈の血栓形成が顕著(HE染色 ×100). |
|
| 35.新生子牛の大腸菌Ο88:H7感染による梗塞性壊死を伴う線維素性化膿性髄膜脳炎 |
| 〔高橋真紀(岩手県)〕 |
交雑種(黒毛和腫・日本短角種),雄,5日齢,鑑定殺.当該例は出生時哺乳困難で,3日齢以降沈鬱,発熱,起立困難,歩様蹌踉,左側眼房水の白濁および泥状便の排泄が観察された.補液や抗生剤は奏効せず安楽殺された.
剖検では,脳脊髄膜に鬱血,点状出血および混濁が観察され,脳脊髄液は混濁し,増量していた.髄膜病変は脳底部で強かった.左側眼球の眼房水は混濁していた.四肢の関節液も混濁し,増量していた.三尖弁,二尖弁および肺動脈の内膜の粗造化,腸漿膜の線維素付着,肝臓の腫大,肺と第四胃粘膜の点状出血ならびに胸腺の萎縮が認められた.
組織学的には,脳脊髄の髄膜,脈絡膜および脳室壁の線維素性化膿性炎が観察され,髄膜病変は顕著だった.病変は鬱血,出血,マクロファージおよび好中球を主体とする細胞浸潤ならびに線維素の析出よりなり,脈絡膜および脳室壁では上衣細胞の剥脱を伴っていた.視床脳および中脳の実質内には,境界やや明瞭な壊死巣が散在性に認められた(図35).壊死病変には神経網の疎鬆化,神経細胞の変性,線維素血栓の多発,出血および好中球とマクロファージの浸潤がみられた.線維素性化膿性炎は左眼球,三尖弁,二尖弁,肺動脈の内膜および腹腔内諸臓器の漿膜にもみられた.これらの病巣に浸潤するマクロファージおよび好中球の細胞質内あるいは細胞外に無数のグラム陰性桿菌が認められ,抗大腸菌Ο88ウサギ血清(動物衛生研究所)を用いた免疫染色により陽性を示した.そのほか,肺の多発性巣状出血,肝細胞の変性,真菌感染を伴う第四胃潰瘍,小腸絨毛の短小化・融合および胸腺の萎縮が観察された.
病原検索では,肝臓,大脳,脳幹および脳脊髄液よりおのおの有意な菌数の大腸菌Ο88:H7が分離された.血液生化学検査では,当該例の放血殺時の血清IgG含量は0.19g/dlであった.
本例は大腸菌Ο88:H7感染に起因する新生子牛の髄膜脳炎と診断された. |

| 図35 |
子牛の間脳における線維素性化膿性脳炎像と神経網の疎鬆化がみられる(HE染色 ×100). |
|
| 36.牛の小脳虫部の軟化と萎縮 |
| 〔尾崎裕昭(鳥取県)〕 |
黒毛和種,雄,1日齢,鑑定殺.繁殖哺育農家で,分娩予定より7日早く生まれた子牛が起立不能であった.発育良好だが眼裂がやや小さく,右眼球瞳孔は散大していた.哺乳能力はあったが,予後不良として2001年5月30日に鑑定殺された.母牛は異常産3種混合ワクチンを接種済みであった.
剖検では,大孔開大と小脳ヘルニアを認め,小脳の尾側は圧迫されて矮小となり,小脳虫部は舌状であった.心嚢水は血様で,脾臓は軽度に腫大していた.
組織学的には,主病変は小脳にあり,虫部にプルキンエ細胞の乏血性変化,壊死,消失および空胞形成,時に石灰沈着,篭形成(empty basket)を認め,顆粒細胞脱落,顆粒層から髄質の疎性化,泡沫細胞浸潤がみられた(図36).虫部錘体断離部では髄質に軸索膨化,淡褐色泡沫細胞浸潤が認められた.小脳矮小部位の下部にあたる延髄領域では両側性に灰白質背角に軟化巣がみられた.大脳側頭葉と頭頂葉境界,後頭葉の限られた領域にび漫性に皮質神経細胞の乏血性変化,髄質神経網の疎性化が認められた.その他の臓器にはび漫性肝細胞脂肪変性,脾臓の濾胞リンパ球減少と傍濾胞領域の軽度好中球浸潤,心内膜下の出血,部分的肺胞虚脱と気管支肺胞腔内軽度好中球浸潤,回腸粘膜上皮細胞の空胞変性,脊髄に軽度硬膜下出血を認めた.
病原検索では,主要臓器から細菌は分離されなかった.
以上から,キアリ型奇形と診断された.本症例では後頭骨大後頭孔の開大と小脳ヘルニア以外に奇形を認めず,小脳病変部の軟化が顕著なことが特徴的であった. |
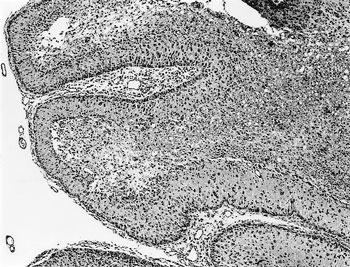
| 図36 |
プルキンエ細胞の壊死や消失,顆粒細胞の脱落,顆粒層から髄質にかけての疎性化や泡沫細胞の浸潤がみられる(HE染色 ×50). |
|
| 37.牛の小脳低形成 |
| 〔長石貞保(奈良県)〕 |
交雑種,雄,13日齢,鑑定殺.2001年2月,起立不能に陥った子牛が後弓反張を呈したため,予後不良と判断し鑑定殺した.食欲などに異常は認められなかったが,逆子のため分娩は難産であった.母牛には異常産3種混合ワクチンが接種されていた.
剖検では,小脳は著しく小さく,軽度に水腫性であった.また,膀胱周囲には分娩時に形成されたと思われる出血および水腫が認められた.体形異常は認められなかった.
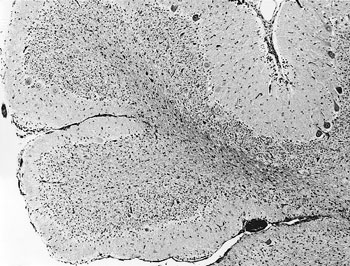
組織学的には,小脳の低形成が認められた.すなわち,小脳皮質の分子層から顆粒層にかけて著しく菲薄化しており,脳回が狭くなって小脳回症を呈していた(図37).プルキンエ細胞および顆粒細胞の数は正常に比べ少なかった.その他の組織には著変を認めなかった.
病原検索では,ウイルス分離陰性で,細菌検査でも主要臓器から細菌は分離されなかった.初乳摂取後の血清抗体価は,アカバネ64倍,アイノ32倍,チュウザン128倍および牛ウイルス性下痢128倍であった.RT-PCR法による検査では,脾臓から牛ウイルス性下痢・粘膜病ウイルス遺伝子は検出されなかった.
本症例は疫学的背景などから牛ウイルス性下痢・粘膜病が疑われたが,持続感染牛ではないと考えられた.母牛のペア血清または子牛の初乳摂取前の血清は採取されていなかったため,確定診断には至らなかった. |
|
| 38.牛の脊髄の神経細胞に認められたPAS・LFB陽性細胞質内封入体形成 |
| 〔安食 隆(島根県)〕 |
黒毛和種,雄,5日齢,死亡例(死後約6時間).当該牛は約2週間の出産遅延で出生時の体重は50kg,体高は85cmであった.神経症状は認めなかった.生後5日目の朝,急に元気消失して斃死した.
剖検では,腹腔および胸腔内に漿液が少量貯留し,脾臓周囲を中心にフィブリンの析出がみられた.肺はうっ血し,左側第4〜第7肋骨部と右大腿部から腰部にかけて出血を認めた.
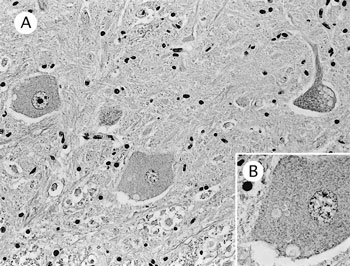
組織学的には,脊髄の神経細胞の細胞質内にさまざまな大きさと個数の封入体を認めた(図38A).細胞質内封入体は,大型神経細胞では比較的大型の有芯空胞として(図38B),小型神経細胞では小型の顆粒状物として認められた.大型の封入体はHE染色直後にはエオジン好性に染まり,周囲にハローを持った構造として認められたが,1日後には染色性が低下した.また,封入体はLFB陽性,凍結切片でPAS陽性,オイル赤Ο陰性,ギムザ染色陰性であった.延髄や大脳基底核などにおいても,同様の所見がみられた.電顕では,封入体は膜様物の同心円状集積または層板状集積として認められたが,これらの構造物を包む膜様構造ははっきりしなかった.その他,肺で強い肺胞水腫,肝臓で肝細胞の空胞変性および胆小管の軽度増数,胸腺で皮質の菲薄化を認めた.
生材料は採取していなかったため,生化学的検査はできなかった.
本症例は封入体の中枢神経系における出現の仕方,特殊染色の性状および超微形態像から蓄積症が疑われたが,生化学的に蓄積物質の同定や酵素欠損の証明はできなかった. |
| 図38 |
A:神経細胞の細胞質内封入体(HE染色 ×200);B:同部強拡大(HE染色 ×400). |
|
| 39.豚の脳室拡張,軟化巣および石灰沈着を伴った非化膿性脳炎 |
| 〔田中宏一(香川県)〕 |
LW種,雄,2日齢.母豚650頭,種雄豚30頭,肥育豚7,500頭を飼育する一貫養豚農家で1998年8月に異常産が続けて3腹に発生したため,8月24日に出生した13頭(死産7,虚弱3,正常3頭)のうち虚弱子豚3頭を病性鑑定した.本症例はそのうちの1頭である.母豚は初産で,豚コレラ・日本脳炎ワクチンは接種されていたが,豚パルボワクチンは未接種であった.
剖検では,大脳軟膜は水腫性で,充血および斑状白色巣が散在していた.脳室は拡張し,無色透明な脳脊髄液の貯留を認めた.腎臓の点状出血,膀胱粘膜の水腫および点状出血もみられた.胃および小腸内容物は黄褐色泡沫状であった.
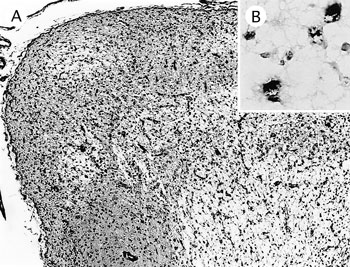
組織学的には,大脳では脳室が拡張し,皮質中層から髄質にかけて疎鬆化および軟化巣が認められた(図39A).軟化巣では脂肪顆粒細胞の浸潤や石灰沈着が認められた.病巣内やその周辺では神経細胞の変性および石灰化も散見され,グリア細胞のび慢性増殖および集簇巣もみられた.また,血管の増生,うっ血および出血とヘモジデリン貪食マクロファージの浸潤,小血管の血管壁に顆粒状の石灰沈着が認められた.髄膜には軽度のリンパ球浸潤がみられた.中脳では中心管の拡張と神経細胞の乏血性変化およびグリア細胞の集簇が,脊髄ではグリア細胞の集簇がみられた.抗豚パルボウイルス抗体(VMRD)を用いたSAB法では,病変部のグリア細胞および脂肪顆粒細胞の細胞質内に陽性反応がみられた(図39B).肝臓では血管内皮細胞の腫大,皮膚では皮下織の水腫およびリンパ球の浸潤が認められた.
血清学的検査では,野外株に感染した母豚の初乳摂取によると思われるパルボウイルス抗体価の上昇が認められた.
以上の所見から,本症例は豚パルボウイルス病と診断された.従来報告されていた非化膿性脳炎に加え,軟化や石灰化がみられたのが特徴的であった. |
| 図39 |
A:皮質の軟化巣と髄質の疎鬆化(HE染色 ×50);B:病変部の豚パルボウイルス抗原陽性細胞(SAB法 ×400). |
|
|