総 説
炭疽菌と生物兵器
6.炭疽菌の病原因子 |
|||||||||||||||
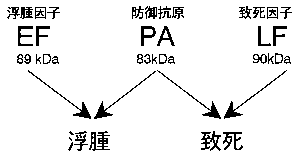
| 炭疽菌の病原因子としては,毒素産生能と莢膜形成能の2つが知られている.毒素産生能は3種類の異なる蛋白,防御抗原(protective antigen,PA;83kDa),致死因子(lethal
factor, LF;90kDa),浮腫因子(edema factor, EF;89kDa)から成っている.LFとEFが毒素の本体であるが,単独では毒性を示さず,PAの存在が不可欠である(図2).また,多くの病原菌では多糖体から成っているのとは異なり,炭疽菌の莢膜は,D-グルタミン酸のホモポリペプチドから成っている.両者の遺伝子支配は,それぞれ強毒株の持つ182および96キロベースの大プラスミドによる.それぞれのプラスミドが,炭疽の病原性に必須であることが証明されており,どちらかが脱落すると毒力が減弱する.パスツールによって作られた炭疽菌の弱毒ワクチン株は,莢膜形成プラスミドの脱落変異株であった. 毒素の細胞内侵入過程は特徴的で,まず,PAが大半の動物細胞上の存在するレセプターに結合する[3].このレセプターが最近同定されている.結合したPAは,細胞表層のプロテアーゼであるフリン(furin)などにより1個所で切断され,細胞表層に結合状態の63kDa(PA63)と細胞表層から遊離する20kDa(PA20)の2つに分かれる.PA63は,LFまたはEFと結合しオリゴマーを作り,細胞内に取り込まれ,細胞に障害を与える.このシステムを利用して,遺伝子組換え技術によりキメラ蛋白を作成して,生理活性物質の細胞内導入やワクチン開発への応用が期待されている[1]. 一方,炭疽菌の莢膜は,免疫学的には“納豆のネバネバ”と同一であり,宿主による免疫機構,特に貪食作用から菌体を守る働きをしていると考えられている. |
|||||||||||||||
 |
|||||||||||||||
図2 炭疸毒素成分 |
|||||||||||||||
7.生物兵器としての炭疽 |
|||||||||||||||
| 7-1.生物兵器の歴史[2] | |||||||||||||||
|
|||||||||||||||
| 7-2.炭疽菌の生物兵器としての利点 | |||||||||||||||
|
|||||||||||||||
 |
|||||||||||||||
7-3.炭疽菌による生物テロのシナリオ |
|||||||||||||||
|
|||||||||||||||
8.炭疽の予防や防御 |
|||||||||||||||
| 炭疽の自然発生を予防するには,炭疽を発症した動物を的確に淘汰し,汚染物の的確な廃棄や殺菌,感受性動物のワクチン接種,感染の可能性のある人間へのワクチン接種が最も効果がある防御方法である. 動物に対するワクチンは無莢膜変異株の芽胞体菌の50%グリセリン加生理食塩水内にアジュバントとして0.5%サポニンが加えられたものがわが国では用いられている.しかし,この株は完全に非病原株であるとはいえず,羊やラマなどには毒力を保持している.また,防御効果は約1年は継続するので,発生地域ではブースターが必要である.一方ヒトに対するワクチンは,中国やロシアでは動物同様芽胞体による生ワクチンが使用されているが,一般的には,莢膜非産生,毒素産生株の上清の明礬沈殿物や水酸化アルミニウム沈殿物が用いられている.しかしヒトへのワクチンは長期間必要であり,副作用もあり,特殊な場合を除いては一般市民には用いられていない.たとえばアメリカの場合,ワクチン接種は2週間ごとに3回皮下注射し,その後,6,12,18カ月後に計3回皮下接種,次に1年おきにブースター接種を皮下に行うよう決められている.そのため,もっぱら動物に対するワクチンにより炭疽を減らそうとしているのが現状で,ヒトへの効果的で副作用の少ない新しいワクチン開発も行われている.しかし,テロリズムを想定した効果的な予防方法は現在のところないが,炭疽菌に暴露された近郊では予防的に抗生物質投与が行われる. |
|||||||||||||||
9.炭疽の抗生物質による治療 |
|||||||||||||||
| 炭疽菌は一般的にペニシンに対して感受性があるので,ペニシリンが第一選択肢として使用される.200万単位のペニシリンを2時間ごと静脈内注射するが,その他テトラサイクリンやエリスロマイシンも使える.耐性菌を考慮すると,シプロフロキサシン(400mgの8〜12時間ごと静注)やドキシサイクリン(初回200mg,その後12時間ごとに100mg静注)がアメリカでは用いられている.ただしこの濃度はアメリカ人を想定したもので,わが国でそのまま適応できるか不明である.また,シプロフロキサシンは2001年11月現在保健薬の適応を受けていない.ショックの回避や補液,酸素吸入などの対症療法も必要である.また,治療や検死中に使用した場所や器具などは,芽胞体の除染が必要である.消毒薬としては,ホルマリンや次亜塩素酸などを殺菌濃度で使用するが,次亜塩素酸は有機物の存在で活性が低下する.過酸化水素水や過酢酸も効果がある. |
|||||||||||||||
10.お わ り に |
|||||||||||||||
| 1857年コッホが炭疽菌を病原菌として同定して以来1世紀半が経とうとしている.この間,炭疽菌は,病原菌の持つあらゆる面を経験して今日にいたっている.炭疽菌の病原因子の一つが莢膜であることは,1908年に報告されている.パスツールが弱毒ワクチン株を作製して,十数年経った頃である.それに遅れること,約20年後,炭疽菌の毒素の存在が報告された.その他の病原因子が同定されてはいるが,おもな病原因子は今なお莢膜と毒素である.単純な因子であると思われるのに,その働きについてはずっと不明のままであった.しかし,この1〜2年,炭疽菌の発症機構の基礎研究が進展し始め,両病原因子とも複雑な機構を持っていることが明らかとなってきている.病気としてはもう古いという見方もあるが,宿主-寄生体の関係からみると,まだまだ興味深い点が少なくない.その一方で,炭疽茵は生物兵器の最有力候補として長く脅威の的であった.その脅威がまさにアメリカで現実に起こってしまった.化学・核兵器と異なり見えない脅威である生物兵器にわれわれはどのように立ち向かえばよいか,真剣に考えなければいけない時代になったのかもしれない. |
|||||||||||||||
引 用 文 献
|